药品审评中心公示2012年1至6月审评任务完成情况及审评结论
为进一步加强公开透明力度,药品审评中心继年初公示化药月审评任务后,2012年7月10日,对上半年审评任务完成情况及其结论再予公示。同时,公示也增加了上半年中药和生物制品的完成情况。
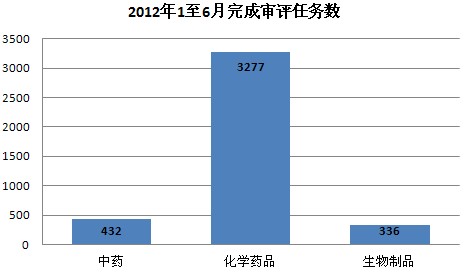
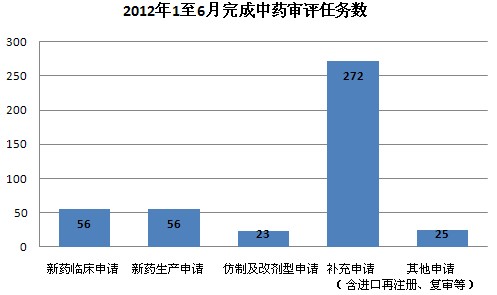
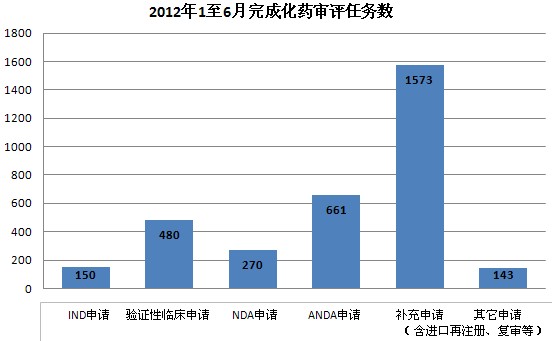
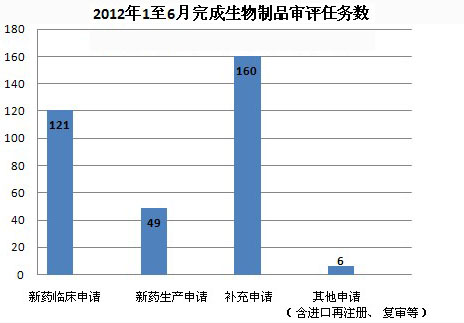
2012年1至6月,药品审评中心完成审评任务共计4045个(以受理号计,非化合物。完成任务中包括补充资料),其中中药432个,化药3277个,生物制品336个。中药审评任务中,新药临床申请56个、新药生产申请56个、仿制及改剂型申请23个、补充申请272个、其它申请(含进口再注册、复审等)25个;化药审评任务中,IND申请150个、验证性临床申请480个、NDA申请270个、ANDA申请661个、补充申请1573个、其它申请(含进口再注册、复审等)143个;生物制品审评任务中,新药临床申请121个、新药生产申请49个、补充申请160个、其它申请(含进口再注册、复审等)6个。
本次审评任务完成情况分别按照中药、化药和生物制品各审评序列进行公示,任务完成统计时间点以完成技术审评、按照中心授权签发的时间为截止点。公示内容包括各具体品种的完成月份、审评任务序列、受理号、本轮任务启动时间、任务首次进入中心时间、本轮任务审评结论等。另外,在相关品种项下,标注了在审评过程中与注册申请人的沟通情况信息。
(摘自:CDE网站 2012-07-10)



 首页
首页 最新动态
最新动态 机构简介
机构简介 国际交流
国际交流 关于我们
关于我们 京公网安备 11010802027110号
京公网安备 11010802027110号