2020年3月17日、国家医薬品監督管理局は「2019年医療機器登録業務報告書」を発表した。その抜粋は以下のとおりである。
2019年、国家医薬品監督管理局は習近平新時代中国特色社会主義思想をガイドラインとし、「4つの『最厳格』」を徹底的に実施し、国民の医療機器安全使用を保障、促進することを使命とし、医療機器審査承認制度の改革を引き続き深化し、監督管理に関する研究を推進し、リスク制御に注力し、責任遂行を強化し、医療機器登録審査承認のクオリティと能率を高めた。
一、医療機器登録業務の実施状況について
(一)医療機器登録管理法規システムのさらなる整備
1、「医療機器監督管理条例」の改正を積極的に推進した。司法部と協力して重点問題に関する現地調査と研究を展開し、条例をさらに改正して改善し、条例の附則と規定類文書の制定と改正を同時に行った。
2、「オーダーメイド型医療機器監督管理規定(試行版)」(2019年第53号公告)を発布した。オーダーメード型医療機器の定義、登録、設計、加工、使用、監督管理などに関する要求事項を明確化し、オーダーメード型医療機器のイノベーションと開発をより推奨し、希少とする個性的な臨床ニーズを満たした。
3、医療機器技術審査ガイドラインの制定と改正を持続的に推進した。「医療機器条件付き上市許可ガイドライン」など57件の医療機器技術審査ガイドラインを公布し、審査基準を統一化し、各級医薬品監督管理部門の審査水準を引き上げた。
(二)医療機器審査承認制度改革の持続的深化
1、臨床試験承認を最適化した。「医療機器臨床試験承認手順の調整に関する公告」(2019年第26号公告)を発表し、臨床試験承認手順をさらに最適化し、「明示」承認から「黙示」承認に変更した。
2、臨床試験免除医療機器目録をさらに増大した。「増補改訂版臨床試験免除医療機器目録の公布に関する公告」(2019年第91号公告)を発表し、148品目の医療機器類製品と23品目の体外診断用試薬類製品が新たに臨床試験免除と決定され、48品目の医療機器類製品と4品目の体外診断用試薬類製品の名称と説明文を修正することになった。現在、臨床試験免除医療機器目録が1003品目、体外診断用試薬目録が416品目で、合計1419品目に達した。
3、イノベーション医療機器の承認業務を円滑に実施した。2019年、36品目のイノベーション製品と12品目の優先承認製品が「グリーン通路」経由で承認を受けた。 陽電子放射断層撮影および磁気共鳴画像診断装置など19品目のイノベーション医療機器、中空糸膜血液透析フィルターなど10品目の優先上市を承認し、医療機器産業の革新的発展を促進し、国民の高水準医療機器使用ニーズを満たす。
4、医療機器登録者制度の試行を拡大した。「国家薬監局による医療機器登録者制度の試行大に関する通達」を発表し、医療機器登録者制度の試行を北京市、江蘇省、浙江省など21の省、自治区と直轄市で推進した。2019年、22社の93製品が登録者制度試行によって承認され、省を跨る委託生産と第三類医療機器登録者制度による委託生産なども含まれる。医療機器登録者制度のメリットをさらに活かし、医療機器イノベーションを奨励し、主体責任の遂行を促進し、医療機器登録者制度の全面的な実施をサポートする。
(三)医療機器に関する基本業務の確実な実施。
1、医療器械標準システムはより整備した。2019年、国家医薬品監督管理局は108件標準の制定と改正を発表した。そのうち、国家標準が15件、業界標準が93件だった。また、業界標準のうち、72件が発表された。2019年末の時点で、既存の医療機器関係有効標準が1671件だった。そのうち、国家標準が220件、業界標準が1451件、中国標準と国際標準の一致度が90.4%に達した。
2、分類と命名業務も引き続き改善された。コンビネーション製品属性判定作業を最適化し、「コンビネーション製品属性判定関係事項の調整に関する通達」を発表し、目録動的調整手順を制定した。3回に分けて1073件の分類判定結果を発表し、正確な分類に関する指導を行った。「医療機器一般名称命名ガイドライン」を公布し、医療機器の一般名称をより規範化させた。
(四)医療機器デジタル監督管理の効果が現れ始め。
1、電子登録を推進した。「医療機器電子登録の実施に関する公告」を発表し、電子登録情報システム(eRPS)を構築し、登録申告のオンライン対処を実現した。2019年、7512件の登録申請がオンラインで行われた。
2、書類審査を実施した。審査業務をデジタルツールで割り当て、簡単項目と複雑項目をランクで分けて審査し、初登録、複雑変更と臨床試験の書類審査を実施し、臨床を目標とする段階別審査評価制度と複雑項目管理者制度を徐々に確立した。
3、医療機器唯一表記制度を実施した。「医療機器唯一表記システム規則」と関連基準を発布し、医療機器唯一表記データベースの1期工事を完了し、製品に「電子身分証」を付与した。原始コードの発行を強化し、生産から臨床使用までのチェーン全体連動を模索した。国家衛生健康委員会と共同で「医療機器唯一表記システム試行実施案」を発表し、共同で試行を実施した。第一陣の医療機器唯一表記業務関係事項を公告し、品目、進捗状況、業務要項を明確化し、医療機器唯一表記業務が各段階で秩序正しく展開されるよう推進した。
(五)臨床試験と登録資料の管理が引き続き強化。
1、医療機器臨床試験への監督と査察を引き続き実施した。20の医療機器臨床試験項目を2つのグループに分けて監督と査察を行い、16の登録項目に対して臨床試験サンプル信憑性延長査察を実施した。
2、医療機器臨床試験実施機構の登録を積極的に推進した。2019年末まで、全国で839カ所の臨床試験機構が登録していた。管理者、プロジェクト責任者と臨床試験技術者を対象に3回にわたって研修を実施した。
3、虚偽資料を提供して登録する行為を厳しく取り締まった。関係情報と手がかりによって、深セン莱福百泰医療科技有限公司に対して査察を実施し、同社が電子版資料を提出して行った上部消化管内視鏡と下部消化管内視鏡の2製品の登録申請を不許可とした。
(六)監督管理の研究を着実に推進。
1、監督管理の研究を積極的に推進した。中国医薬品監督管理科学的行動計画を実施しはじめた。第一陣としてスタートしたプロジェクトは、コンビネーション製品の評価と研究、人工知能(AI)活用医療機器の安全性と有効性評価と研究、医療機器関連新材料監督管理と研究、リアルワールドデータを医療機器臨床上評価に用いる方法学研究などのプロジェクトである。四川大学、華南理工大学で、国家医薬品監督管理局監督管理科学研究拠点を設立し、医療機器監督管理の研究を推進した。
2、医療機器臨床関係リアルワールドデータ応用の試行を推進した。監督管理科学的行動計画に合わせて、臨床関係リアルワールドデータ応用の試行を推進し、重点地域に依拠し、試行案を制定し、試行対象を確定し、「医療機器臨床上評価における臨床関係リアルワールドデータ応用技術ガイドライン」を制定した。
(七)国際交流と協力における効果向上。
1.国際交流で多くの成果をあげた。国際医療機器規制当局フォーラム(IMDRF)第16回管理委員会会議に参加し、会議では、IMDRF加盟国全員の同意を得た上で、我国がリードする臨床評価グループによる「臨床的証拠-重要な定義と概念」、「臨床評価」、「臨床研究」という3つのガイドラインが承認された。我国のIMDRF加盟後、我国の医薬品監督管理部門が主導してガイドラインを作成したのは今回が初めてである。管理委員会は同時に、我国がリードして制定した「市販後臨床フォローアップ」プロジェクトの立ち上げに賛成した。また、管理委員会では中国が国家監督管理部門報告情報交換メカニズムへの参加を満場で同意された。加盟国と医療機器類製品に関する安全情報を共有し、グローバルな医療機器リスク課題に共同で対応することを目指す。また、中国は標準関係業務チームの議長国として、会議で管理委員会と関係業界に標準関係業務チームの業務実施状況と進展を紹介された。研究成果としての「認可基準と使用状況分析報告書」と「認可基準リスト」は管理委員会の全員一致で可決された。
2、第24回アジア医療機器規制協調会議(AHWP)年次総会に参加した。AHWP副主席と2つの業務チームの主席として、医療機器登録と監督管理システムの最新進展を紹介し、業務チームの議論と法規関係協調業務を司会し、中国の地域医療機器監督管理における役割を十分に発揮し、アジアの法規協調業務を積極的に推進した。
二、医療機器登録申請における受理状況について
2019年、国家医薬品監督管理局は職責を果たし、医療機器初登録、登録延長と許可事項変更申請を9104件受理し、2018年と比べて37.8%増えた。
(一)全体状況
受理された国内第三類医療機器登録申請が3511件、受理された輸入医療機器登録申請が5593件だった。
品目別でみると、医療機器登録申請が5877件、体外診断用試薬登録申請が3227件だった。
登録類別でみると、初登録申請が1693件で、医療機器登録申請全体の18.6%を占め、登録延長申請が5081件で、全体の55.8%を占め、許可事項変更申請が2330件で、全体の25.6%を占めた。登録類型の割合は下図を参照するように。
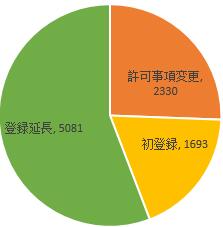
図 登録受理項目における登録類別割合図
初登録1693件 登録延長5081件 許可事項変更2330
三、医療機器登録における承認状況について
2019年、国家医薬品監督管理局が承認した医療機器初登録申請、登録延長申請と変更申請が合計8471件で、2018年と比べて53.2%増えた。そのうち、初登録申請が1726件、登録延長申請が4504件、許可事項変更申請が2241件だった。
2019年、企業が自ら撤回した医療機器登録申請は210件で、自ら取り消した登録証が66件だった。
最近6年間における医療機器登録の承認状況については、下図を参照するように。

図 2014-2019年登録の承認状況
(一)全体状況
2019年、国家医薬品監督管理局が承認した国産第三類医療機器登録申請は合計3179件で、2018と比べて86.0%増加した。また、承認した輸入医療機器登録申請は合計5292件で、2018年と比べて38.6%増加した。
承認された登録品目別でみると、医療機器関係が5226件で、全体の61.7%を占め、体外診断用試薬関係が3245件で、全体の38.3%を占めた。
承認された登録類別でみると、初登録申請が1726件、登録延長申請が4504件、許可事項変更申請が2241件だった。それぞれ全体の20.4%、53.2%、26.4%を占めた。各登録類別の内訳は下図を参照するように。
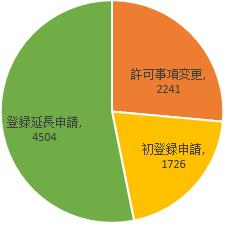
図 2019年承認された登録申請類別割合図
初登録申請 1726件 登録延長申請 4504件 許可事項変更申請 2241件
四、イノベーション医療機器などの製品の承認状況について
2019年、国家医薬品監督管理局は、「イノベーション医療機器特別審査手順」に基づき、イノベーション医療機器の審査業務を引き続き円滑に実施し、合計179件のイノベーション医療機器特別審査実施申請を受理し、36件のイノベーション医療機器特別審査プログラムに入られた。31件の優先審査申請を受理し、そのうちの12件に対して優先承認を認可し、合計で19品目のイノベーション医療機器の上市を承認した。
五、その他登録管理の状況について(略)
注:本報告書におけるデータの統計期間は2018年1月1日から2019年12月31日までである。
(出所:国家医薬品監督管理局サイト2020-03-17)



 ホーム
ホーム 最新情報
最新情報 機構紹介
機構紹介 国際交流
国際交流 サイトについて
サイトについて