2017年5月31日、国家食品医薬品監督管理総局は「2016年医薬品査察報告書」を発表した。当該報告書は中国語版と英語版があり、2016年医薬品査察実施状況および査察で発覚した主な問題を述べ、各種査察で発覚した弱点と潜在的なリスクを分析した。また、当該報告書は7節によって構成される。各節のタイトルは順番で医薬品登録関係生産現場査察、医薬品GMP認証査察、医薬品GMP追跡査察、医薬品抜き打ち査察、輸入医薬品関係海外査察、医薬品流通査察と海外機関によるGMP関係査察である。
2016年各種完了査察リスト
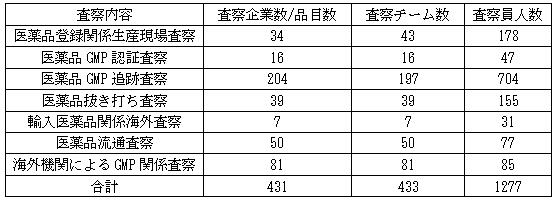
関連リンク:2016年医薬品査察報告書(中国版?英語版)
(抜粋)
第五節 輸入医薬品関係海外査察
一、査察の基本状況
(一)年間査察任務の概要
総局による「2016年輸入医薬品関係海外生産現場査察計画の実施に関するお知らせ」などの書類に基づき、2016年に実施した海外査察は合計49件だった。
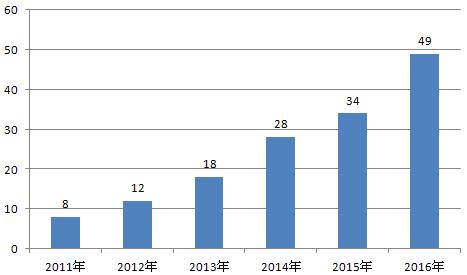
図5-1 2011-2016年における海外査察件数
1、2016年の査察任務は19カ国にわたって実施された。そのうち、ヨーロッパ、北米などのエリアで査察を実施する品目が多く、医薬品品質リスクが高いインド、ベトナムなどの国々で査察を実施する品目もある程度の割合を占めた。また、南米とオーストラリアでの査察にも力を入れた。
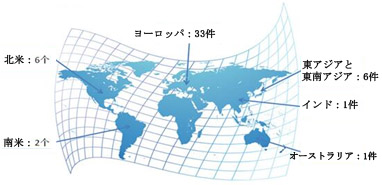
図5-2 2016年各国における査察任務について
2、「査察は審査承認にサポートする」という原則に従い、上市製品の安全性要求事項も考慮に入れ、審査中品目に関する査察の割合を増やし、臨床申請、生産申請、再登録申請と補充申請を行う製品をいずれも査察の対象とした。また、上市済み製品に対する査察を行う原因は、主に港湾における査察で品質問題を発覚したこととハイリスク製品の副作用モニタリング拡大にある。
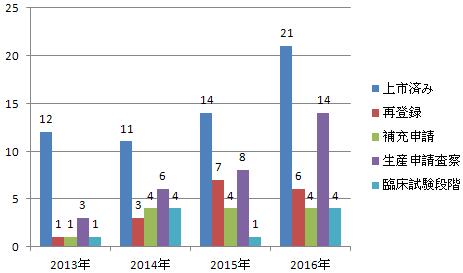
図5-3 近年における査察任務の実施状況
3、今回は査察対象になった品目が幅広く、剤型も多いといった特徴があり、化学医薬品製剤に対する査察にも力を入れた。査察対象になった化学医薬品は40品目に達し、注射剤、固体製剤、植え込み剤、鼻スプレーなどを含んだ。そのうち、バイオ医薬品は3品目、原薬は6品目、ワクチン、血液製品と治療用バイオ製品は11品目、植物由来薬品は4品目だった。
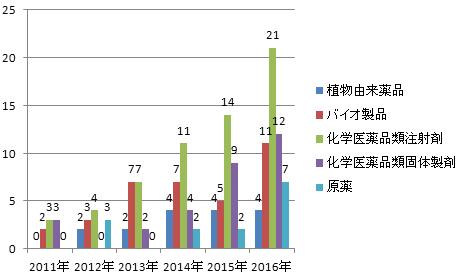
図5-4 査察任務の分類状況
(二)2016年査察実施状況
総局が年度中業務計画に従い、2016年の海外査察実施時間を調整し、生産企業の生産スケジュールの調整にもあたって、2016年は合計15品目に対する査察を完了した。そのうち、7品目は現場査察が行われ、3品目は不合格で、全体の42%を占めた。8品目は査察準備期間中、企業が自ら関係品目の輸入登録証を取り消し、もしくは審査請求が却下されたといった結果になり、全体の17%を占めた。なお、21品目は企業による生産スケジュール調整で、2017年第1四半期に査察を行うことになり、12品目は企業が2017年第1四半期に査察を受けることができないため、2017年海外査察計画に編入された。
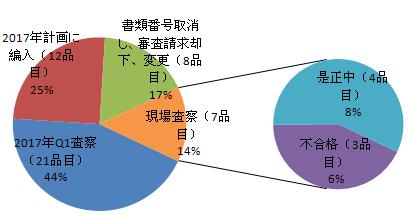
図5-5 2016年査察実施状況
2017年Q1査察(21品目)44% 2017年計画に編入(12品目)25% 書類番号取消し、審査請求却下、変更(8品目)17% 現場査察(7品目)14% 是正中(4品目)8%
不合格(3品目)6%
二、海外査察で発覚した主な問題
査察完了の7品目のうち、3品目は不合格で、不合格率は往年より高くなった。査察で発覚した欠点は117項目だった。そのうち、重大欠陥は3項目、主要欠陥は18項目だった。問題は主に品質制御と品質保証、原材料管理システム、変更管理などにある。重大欠陥は主に生産手順の一致性およびデータの信憑性に関するものである。海外で発覚した問題は関係法律と規定に基づいて対処する。
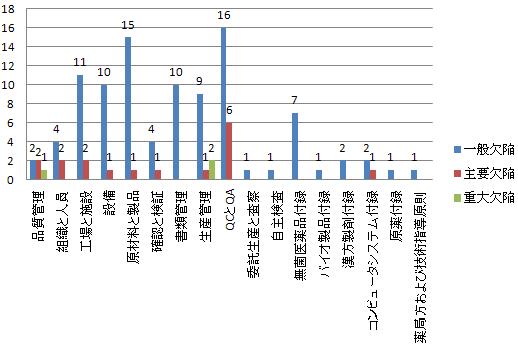
図5-6 2016年海外査察で発覚した欠陥のまとめと分析
主要及び重大問題は以下のとおりである。
1、生産手順、生産場所などは登録申請時の記述と異なり、重大変更などは事前に申請せず、無断で実施されたこと。
2、データの信憑性には大きな問題があり、製品の品質に大きく影響したこと。
3、現場査察以外の処理された品目が増えたこと。
(出所:CFDAサイト2017-06-01)



 ホーム
ホーム 最新情報
最新情報 機構紹介
機構紹介 国際交流
国際交流 サイトについて
サイトについて