4月28日、国家食品医薬品監督管理総局は「2016年国家医薬品副作用モニタリング年間報告書」を発表した。報告書は4つの部分によって構成され、2016年医薬品副作用モニタリング業務の全体進捗状況、医薬品副作用報告の状況、リスク制御措置の実施状況および5つの注意すべき問題をまとめた。その抜粋は以下のとおりである。
一、医薬品副作用モニタリングの進捗状況
ネットワークの構築がより整備させ、モニタリング能力もより向上した。2016年、国家医薬品副作用モニタリングネットワークの構築がより整備するに伴い、我国の医薬品副作用関係情報の発見と収集能力もより高まった。地方ネットワークのユーザー数は急速に増加し、全国では、31万以上の医療機構、医薬品生産経営企業は医薬品副作用モニタリングネットワークに登録してユーザーになり、当該ネットワークを利用して副作用の報告を行った。全国97.7%の県は医薬品副作用を報告し、人口百万人あたりの報告件数は1068件に達し、2015年より増加した。
分析と評価能力は引き続き向上し、リスク管理とコミュニケーションも円滑に行われた。2016年、医薬品副作用報告とモニタリングに関する業務は秩序正しく実施された。日間モニタリング、週間総括、四半期毎分析などの方法で国レベル医薬品副作用モニタリングデータの分析と評価に力を入れ、医薬品リスクの兆しを発覚し、テストステロン含有医薬品、フェナセチン含有医薬品、注射用ビダラビンリン酸、複方大青葉錠、複方アミノ酸注射液(18AA)および同類製剤、仙霊骨葆内服製剤など42品目の医薬品に対する安全性評価を行い、関係リスク管理とコミュニケーション措置をとった。また、安全性評価の結果に基づいて35件の添付文書修正提案を行った。医薬品副作用関係情報の公開を4回行った。「医薬品警戒速報」を12期刊行し、68品目に関する63件の情報を伝達した。クロルメザノンとフェンホルミンの2品目に関する公告を撤回した。
副作用モニタリングを引き続き強化し、早期警報業務の能率を高めた。医薬品副作用関係兆しへの対処を規範化させ、早期警報プラットフォームの確立に力を入れ、早期警報業務の能率を高め、150件以上の医薬品副作用の兆しを発覚して速やかに処置し、黄体ホルモン注射液など6つの事件に関するリスク制御措置をとり、公衆が安全に医薬品を使用するようより保障した。
企業による主体的責任の遂行を引き続き促進し、医薬品安全保障の水準をより高めた。2016年、企業における医薬品副作用モニタリングに関する研修に力を入れ、医薬品生産企業の責任意識と医薬品安全性評価能力向上を推し進めた。医薬品生産企業に副作用モニタリングデータを提供し、関係企業がデータ分析と評価を行い、リスク制御措置を速やかにとるよう指導し、関係企業が主体的責任を果たすよう促した。
二、医薬品副作用/事件報告の状況
(一)全体状況
1、2016年における医薬品副作用/事件報告の状況
2016年、全国医薬品副作用モニタリングネットワークが受け付けた「医薬品副作用/事件報告表」は合計143万件に達し、2015年より2.3%増加した。1999年から2016年まで、全国医薬品副作用モニタリングネットワークが受け付けた「医薬品副作用/事件報告表」は合計1075万件だった。
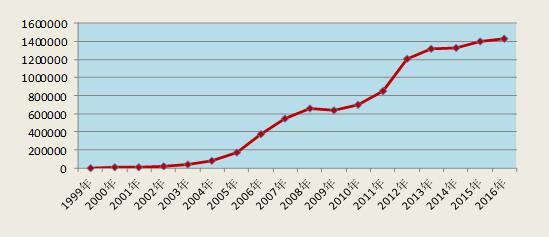
図1 1999-2016年全国医薬品副作用/事件報告件数の増加趨勢
2、新規と重篤医薬品副作用報告の状況
2016年、全国医薬品副作用モニタリングネットワークが受け付けた新規と重篤医薬品副作用/事件報告の件数は42.3万件に達し、2015年より7.4%増加した。新規と重篤報告の件数は同時期報告総件数の29.6%を占め、2015年より1.4ポイント増加した。新規と重篤副作用/事件報告が占める割合の持続的増加は、我国医薬品副作用/事件報告総件数の増加は有意義だと示している。
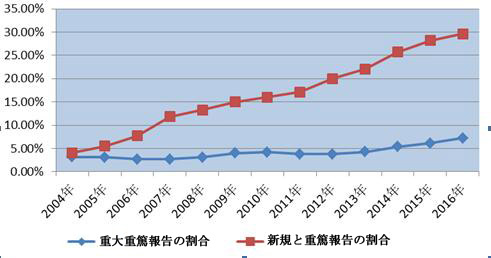
図2 2004‐2006年新規と重篤及び重大重篤医薬品副作用/事件報告件数の割合
3、人口百万人あたりの症例報告状況
人口百万人あたりの症例報告件数は一つの国の医薬品副作用モニタリング水準を判断する重要指標の一つである。2016年、我国では、人口百万人あたりの症例報告件数は1068件、2015年より2.4%増加した。
4、県による医薬品副作用/事件報告の比例
県による医薬品副作用/事件報告の比例は我国医薬品副作用モニタリングのバランスとカバー率を判断する重要指標の一つである。2016年、全国各地の県による医薬品副作用/事件報告の比例は97.7%に達し、2015年より1.1ポイント増加した。
5、医薬品副作用/事件報告の出所
医薬品の生産企業、経営企業と医療機構は医薬品副作用/事件報告の責任者である。2016年における医薬品副作用/事件報告の出所をみれば、医療機構は85.6%、医薬品経営企業は12.8%、医薬品生産企業は1.4%、個人とその他は0.2%だった。
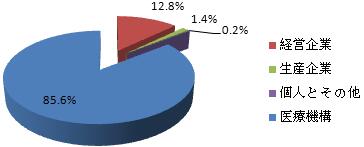
図3 2016年医薬品副作用/事件報告の出所
6、報告者の職業
報告者の職業に関する統計データをみれば、医者は55.5%、薬剤師は25.3%、看護師は15.1%、その他は4.1%だった。報告者の職業構成は2015年とほぼ同様だった。
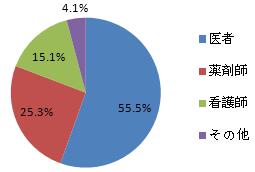
図4 報告者の職業構成
7、医薬品副作用/事件報告にかかわる患者の状況
2016年、医薬品副作用/事件報告にかかわる患者の男女比は約0.89:1。女性は男性より多かったという結果になったが、性別比は2015年とほぼ同様だった。また、14歳以下の児童患者に関する報告は全体の9.9%を占め、2015年と同様だった。65歳以上の高齢患者に関する報告は全体の23.5%を占め、2015年より2.0ポイント上がった。
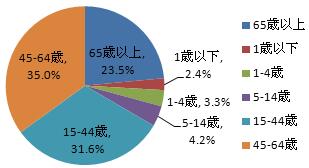
図5 2016年医薬品副作用/事件報告にかかわる患者の年齢構成
8、副作用/事件報告にかかわる医薬品の状況
副作用を疑う報告の類別によって、化学医薬品は81.5%、漢方薬は16.9%、バイオ製品(ワクチン除外)は1.6%で、2015年とほぼ同様だった。
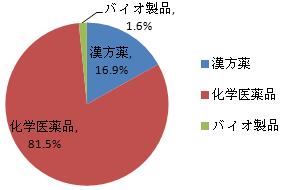
図6 2016年副作用/事件報告にかかわる医薬品の類別
投与ルートで2016年の医薬品副作用/事件報告を分類すれば、静脈注射関係は59.7%、その他注射(例えば、筋肉注射や皮下注射など)関係は3.4%、経口投与関係は33.7%、その他ルート(例えば、外用や貼付など)は3.2%だった。2015年と比べて顕著な変化はなかった。
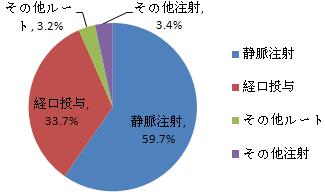
図7 2016年副作用/事件報告にかかわる医薬品の投与ルート
9、器官系損害を及ぼす医薬品副作用/事件の報告状況
2016年、器官系損害を及ぼすあらゆる医薬品副作用/事件の報告で、損害ランキングトップ3は皮膚およびその付属器損害(27.6%)、胃腸系損害(25.4%)と全身損害(10.9%)だった。化学医薬品、漢方薬による損害のトップ3は全体と同様だったが、バイオ製品による損害のトップ3は全体とやや異なり、順番で皮膚およびその付属器損害、全身損害および免疫機能混乱だった。
10、医薬品副作用/事件報告全体状況に関する分析
2016年における医薬品副作用/事件報告の全体状況は2015年と比べて顕著な変化はなかった。
また、医薬品副作用/事件報告の出所をみれば、医療機構による報告は85.6%を占め、2015年と比べて3.4ポイント増加し、医者による報告は55.5%を占め、2015年と比べて1.5ポイント増加した。これは医療機構が医薬品副作用/事件報告の主な出所であることを示している。医薬品生産企業による報告件数は2015年とほぼ同様で、量的には依然として少なく、医薬品生産企業が副作用モニタリングに十分努めていないことを示している。医薬品生産企業は医薬品副作用モニタリングと報告への認識を深め、上市済み医薬品の安全性研究に力を入れ、リスク管理制度を確立し、企業としての責任意識を高め、速やかにリスクの予防と制御を行い、「医薬品安全第一責任者」としての責任を十分果たさなければならない。
(二)必須医薬品モニタリングの状況
1、国レベル必須医薬品モニタリングの全体状況
2016年、全国医薬品副作用モニタリングネットワークは合計で59.5万件の国家必須医薬品副作用/事件報告(報告総件数の41.6%を占めた)を受け付け、2015年より2.0ポイント増えた。そのうち、重篤副作用/事件報告は4.5件で、7.5%を占め、2015年より1.1%増えた。化学医薬品とバイオ製品副作用報告は83.4%を占め、漢方薬副作用報告は16.6%を占めた。
2、国家必須医薬品に属する化学医薬品とバイオ製品副作用/事件報告の状況に関する分析
2012年版「国家必須医薬品目録(末端医療機構使用部分)」における化学医薬品とバイオ製品の部分では、25類別の317品目が収録されている。2016年、全国医薬品副作用/事件モニタリングネットワークは当該目録にかかわる356品目に関する50.2万件の報告を受け付けた。そのうち、重篤報告は4.3万件で、全体の8.5%を占めた。
2016年、国家必須医薬品に属する化学医薬品とバイオ製品の副作用/事件報告を類別によって統計すれば、トップ5は抗感染薬、心血管系用医薬品、抗がん薬、消化器用医薬品、鎮痛?解熱?消炎?抗リウマチ?抗痛風類医薬品に関する報告で、化学医薬品関係報告総件数の72.2%を占めた。
2016年、国家必須医薬品に属する化学医薬品とバイオ製品が器官系損害を及ぼす副作用/事件報告のうち、損害ランキングトップ5を占めたのは皮膚およびその付属器損害(27.4%)、胃腸系損害(27.2%)、全身損害(9.7%)、中枢および外周神経系損害(9.0%)、免疫機能混乱と感染(4.0%)だった。トップ5に関する報告の総件数は副作用/事件報告全体の77.4%を占めた。
3、国家必須医薬品に属する漢方薬副作用/事件報告の状況に関する分析
2012年版「国家必須医薬品目録(末端医療衛生機構配置部分)」における漢方製剤の部分では、内科用医薬品、外科用医薬品、婦人科用医薬品、眼科用医薬品、耳鼻咽喉科用医薬品、整形外科用医薬品という6種類の203品目が収録されている。2016年、国家医薬品副作用モニタリングネットワークは当該目録における203品目に関する9.9万件の副作用/事件報告を受け付けた。そのうち、重篤副作用/事件報告は6857件で、6.9%を占めた。
また、上記6種類漢方薬において、副作用/事件報告件数が最も多かったのは内科用医薬品、その次は整形外科用医薬品、婦人科用医薬品、耳鼻咽喉科用医薬品、外科用医薬品、眼科用医薬品という順番だった。そのうち、内科用医薬品関係報告の件数は報告総件数の85.7%を占めた。これは内科用医薬品の臨床使用量が大きく、且つ必須医薬品目録では漢方注射剤も内科用医薬品に分類されていることに起因しているかもしれない。内科用医薬品のうち、副作用/事件報告の件数がトップ5を占めたのは、打撲傷治療剤、温裏剤、開竅剤、解熱剤、扶正袪邪剤だった。この5品目医薬品の報告件数は内科用医薬品報告総件数の90%を占めた。
2016年、国家必須医薬品目録における漢方製剤の副作用/事件報告のうち、器官系損害にかかわる報告のトップ3は順番で皮膚およびその付属器損害(29.0%)、胃腸系損害(23.4%)と全身損害(14.3%)に関するものだった。剤形別でみれば、注射剤による損害のトップ3は皮膚およびその付属器(21.4%)、全身損害(12.7%)、胃腸系損害(6.5%)で、内服製剤による損害のトップ3は胃腸系損害(16.1%)、皮膚およびその付属器損害(5.1%)、神経系損害(2.6%)だった。
以上のモニタリングデータが示したように、2016年国家必須医薬品副作用/事件報告の全体状況は安定していた。
(三)化学医薬品、バイオ製品副作用モニタリングの状況
全体状況
2016年、副作用/事件報告の中で、副作用を疑われる報告は150.7万件に達し、そのうち、化学医薬品関係は81.5%、バイオ製品関係は1.6%を占めた。また、重篤副作用/事件報告で、副作用を疑われる報告は12.2万件に達し、そのうち、化学医薬品関係は86.9%、バイオ製品関係は1.8%を占めた。
(四)漢方薬副作用モニタリングの状況
全体状況
2016年、副作用/事件報告の中で、副作用を疑われる報告が150.7万件に達し、そのうち、漢方薬関係は16.6%を占めた。また、全国医薬品副作用/事件モニタリングネットワークは合計10.2万件の重篤副作用/事件報告を受け付け、漢方薬関係はそのうちの5.5%を占めた。
三、関係リスク制御の措置
国家食品医薬品監督管理総局は、公衆が安全に医薬品を使用するよう保障するために、2016年における医薬品副作用モニタリングのデータと評価結果に基づき、安全上の潜在的なリスクが発覚された医薬品に対し、リスク制御措置を速やかにとった。
(一)4期の『医薬品副作用情報通報』を刊行し、注射用ビダラビンリン酸による重篤副作用および適応症以外の使用によるリスク、仙霊骨葆内服製剤による肝臓損の傷リスク、テストステロン含有医薬品による心血管疾患のリスク、新複方大青葉の長期、大量使用またはその他同類成分の医薬品同時使用時に起こるひどいじんましん、など重篤副作用への注意を喚起し、医薬品安全使用のためのリスク制御を促した。
(二)ロシグリタゾンおよびその複方製剤、茵栀黄注射液、複方アミノ酸注射液(18AA)および同類製剤など、19種類医薬品の添付文書を修正し、特に添付文書における警告表現や副作用、禁忌症などに関する情報を修正した。
(三)モニタリング結果に基づき、フェンホルミンとクロルメザノンの登録許可書を取り消した。
(四)12期の『薬物警戒速報』を刊行し、アリピプラゾール、センシンレン使用製品、ペグインターフェロンα-2b製剤などに関する海外医薬品安全情報を63件伝えた。それらの情報は68品目にかかわる。
四、各論(略)
(一)抗感染薬
(二)漢方薬と西洋薬の複方製剤
(三)解熱鎮痛消炎薬
(四)向精神薬
(五)小児用医薬品
五、関係説明事項
(一)本報告書におけるデータは2016年1月1日から12月31日までの間に各地域が国家医薬品モニタリングデータベースに提出したものである。
(二)多くの国々と同様に、我国の医薬品副作用/事件報告も報告システムで行われ、データベースに収録されているが、報告漏れ、記入ミス、情報不完全、副作用発生率計算難など、システムの限界も存在している。
(三)医薬品副作用/事件報告の件数が当該品目の使用量と副作用発生率など多くの要因に左右されているため、件数の多寡だけでは、医薬品副作用発生率の高低または深刻度を直接判断できない。
(四)本報告書完成時まで、一部の重篤副作用/事件報告、死亡報告がまだ調査と評価の最中で、本報告書における統計結果はいずれも当時の状況を如実に反映しているが、最終的な結果ではない。
(五)専門家は医薬品副作用/事件の関連性を分析し、医薬品安全性関係リスクの情報をまとめ、リスクの普遍性または深刻度によって、医薬品添付文書に安全性情報を加筆し、もしくは医薬品安全使用の情報を更新するといった関係措置をとるかどうかを決定する。稀であるが、医薬品を使用するメリットがリスクより少ないと思われたため、医薬品の市販を中止する場合もある。
(六)本報告書はワクチン副作用/事件モニタリングのデータを収録していない。
(出所:CFDAサイト2017-04-28)



 ホーム
ホーム 最新情報
最新情報 機構紹介
機構紹介 国際交流
国際交流 サイトについて
サイトについて