2012年5月31日、国家食品医薬品監督管理局は2011年医薬品不良反応モニタリング年間報告書を発布して、医薬品不良報告全体概況、医薬品不良反応/事件報告統計分析、医薬品リスク制御措置総括などの三つの面で年間の医薬品不良反応状況を通達した。
2011年国家医薬品不良反応モニタリング年間報告書
医薬品不良反応とは、合格の医薬品が正常な用法用量の下で現れた医薬品使用の目的と関係ない有害反応を指す。1988年に中国が医薬品不良反応モニタリング制度を試行して以来、医薬品不良反応モニタリングは医薬品安全性の情報を見つけ、医薬品安全に対する監督管理を強化し、臨床における医薬品の安全で合理的な使用を促進し、医薬品のリスクを制御する重要なルートと手段となり、国民の医薬品使用安全を保障するに重要な役割を果たしている。全面的に中国の医薬品不良反応に対するモニタリングと監督管理の状況を反映し、医薬品使用安全のレベルを高め、臨床における合理的な医薬品使用を促進するために、「医薬品不良反応報告と監督管理規則」に基づき、国家食品医薬品監督管理局は2011年医薬品不良反応に対するモニタリングと監督の状況に対して総括分析を行った。
一、2011年医薬品不良反応報告とモニタリングの全体的状況
2011年、全国は計852,799件の医薬品不良反応/事件報告を受け取り、百万人ごとに平均して637件の病例報告があった。その内、新しいと重大な不良反応/事件報告の数は145,769件あり、同期の報告総数の17.1%を占め、2010年に比べるとほぼ同じ水準を保っていた。
2011年医薬品不良反応/事件報告の出所によって統計すれば、医療機構からの報告は83.1%を占め、医薬品生産、経営企業からの報告は13.7%を占め、個人からの報告は3.2%を占めた。医療機構が不良反応報告の主体とする局面は依然として変わらず、医薬品生産、経営企業からの報告の割合は2010年に比べると少々上昇したが、やはり不足であった。
二、2011年医薬品不良反応/事件報告に対する分析
1.化学医薬品の中に感染抵抗系類は依然として一位
(1)全体病例報告が及んだ化学医薬品の類別
医薬品不良反応/事件報告の中、感染抵抗系医薬品報告の数は化学医薬品病例総数の51.2%を占めた。その次は心臓・血管系医薬品は8.5%を占め、消化系医薬品は5.6%を占め、電解質、酸塩基平衡と栄養薬は4.2%を占めた。感染抵抗系医薬品病例の報告数は化学医薬品病例報告数の半分を上回ったが、2010年に比べると1.4パーセンテージ降下した。これは、医療機構の感染抵抗系医薬品を規範的に使用するのを強化することにかかわると考えられる。
(2)重大な病例報告が及んだ化学医薬品の類別
化学医薬品の重大な病例報告の中に、一番よく見かける類別は感染抵抗系医薬品であり、44.9%を占め、2010年に比べると3.6パーセンテージ降下した。その他のトップ五位の化学医薬品の類別はぞれぞれ腫瘍抵抗系医薬品(15.9%を占める)、心臓・血管系医薬品(4.7%を占める)、電解質、酸塩基平衡と栄養薬(4.3%を占める)、神経系医薬品(4.1%を占める)であった。重大な病例報告の中、半数近い報告は感染抵抗系医薬品に及んだ。
(3)感染抵抗系医薬品の具体的な品目のランク
すべての重大な感染抵抗系医薬品報告の中、病例報告の数量が1,000件を超えるのはそれぞれセファロスポリン系(34.8%)、ペニシリン系(14.0%)、ニューキロノン系(12.2%)であった。この三種類の医薬品病例報告の数量は感染抵抗系医薬品総数の61.0%を占め、2010年のランク及び割合とほぼ同じであった。
セファロスポリン系のトップ3の品目はそれぞれセフトリアキソン注射液、スルバクタムナトリウム‐セフォペラゾンナトリウム注射液とセフォタキシム注射液であり、ペニシリン系のトップ3の品目はそれぞれペニシリンG注射液、アズロシリン注射液とアモキシシリン経口製剤であり、ニューキロノン系のトップ3つの品目はそれぞれレボフロキサシン注射液、ガチフロキサシン注射液と塩酸モキシフロキサシン注射液であった。2010年に比べると、2011年のデータには目立った変化がなかった。
2.静脈注射による投薬ルートのリスクは高い
(1)2011年の医薬品不良反応/事件報告の中にある投薬ルートは静脈注射を主として、55.8%を占めた。その次は経口投薬であり、39.3%を占めた。化学医薬品、中成薬の投薬ルートの分布状況は2010年とほぼ同じであった。
(2)2011年の重大な医薬品不良反応/事件報告にある投薬ルートは静脈注射を主として、73.4%を占めた。その次は経口投薬であり、20.0%を占めた。その他の投薬ルートは6.6%を占めた。静脈注射による投薬ルートのリスクが高いことを提示し、合理的な投薬剤型、ルートを選ぶことは、不良反応の発生を減少することにつながる重要な方法である。
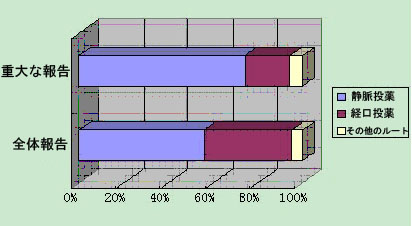
図1 2011年医薬品不良反応/事件の投薬ルートの分布
3.中高年患者の医薬品使用安全に警戒
(1)2011年医薬品不良反応/事件病例報告の中、1歳以下は19,419件、2.3%を占め、1~4歳は39,726件、4.7%を占め、5~14歳は38,524件、4.5%を占め、15~44歳は368,440件、43.2%を占め、45~64歳は264,588件、31.0%を占め、65歳及びその以上は122,102件、14.3%を占めた。
(2)2011年重大な医薬品不良反応/事件病例報告の中、1歳以下は743件、2.3%を占め、1~4歳は1,306件、4.0%を占め、5~14歳は1,300件、4.0%を占め、15~44歳は11,212件、34.5%を占め、45~64歳は11,152件、34.4%を占め、65歳以上は6,739件、20.8%を占めた。
全体病例報告の年齢分布に比べると、14歳以下の児童患者の割合はほぼ同じであり、45~64歳患者の割合は上がり、65歳以上のお年寄りの割合は著しく上がったことから、中高年患者の医薬品使用に対する見守りを強化すべきであることを提示した。
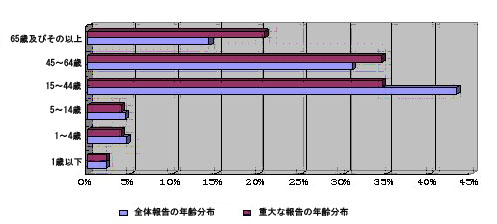
図2 2011年重大な報告と全体報告の年齢分布
4.漢方薬注射液は依然として漢方薬製剤の主なリスク
2011年に全国は漢方薬注射液報告を計65,572を受け取り、その内、重大な報告は4,034件であった。2011年漢方薬注射液報告の中、数量が上位を占める類別は理血剤、補益剤、開竅剤、発汗剤、解熱剤、祛痰剤であり、漢方薬注射液全体報告の97.3%を占めた。2011年漢方薬注射液不良反応/事件報告の中、数量においてトップ3の医薬品はそれぞれ清開灵注射液、双黄連注射液と参麦注射液であった。
分析では、漢方薬注射液の重大な不良反応が末端医療衛生機構での発生は際立っていることを明らかにしたので、末端医療機構は漢方薬注射液の合理的な使用を強化し、慎重に医薬品使用の合併を扱い、不良反応に対する手当をよく運ぶべきであることを提示する。
5.2011年国家基本医薬品の安全状況は安定
2011年、全国医薬品不良反応モニタリングネットワークは国家基本医薬品の不良反応/事件報告を計310,397件を受け取り、その内、重大な報告が11,580件、3.7%を占めた。国家基本医薬品報告が及んだ医薬品類別の中に、化学医薬品病例報告の構成割合は2011年全体報告構成状況と2010年基本医薬品報告の構成状況に比べると、目だった差異はない。2011年国家基本医薬品不良反応/事件報告の総数、重大な報告の数量の増長レベルは全体病例報告の増長レベルとほぼ同じであった。2011年国家基本医薬品の安全状況は安定であった。
三、医薬品リスクの制御
2011年、国家食品医薬品監督管理局は医薬品不良反応モニタリングデータに対する分析・評価の基礎を踏まえて、安全性において隠れた危険が見つかった医薬品に対して関係の管理措置をとった。
1.医薬品安全警告の情報を発布:2011年に「医薬品不良反応情報通達」計9期を発布して、9件(種)の医薬品安全性情報を通達した。「医薬品警戒速報」計11期を発布して、60種余りの医薬品安全性情報を通達した。
2.製品取扱書を修正:2011年、国家食品医薬品監督管理局は通知を発布して、生産企業にイソトレチノイン製剤、ニメスリド経口製剤のリスクを取扱書で明確に提示し、広範なる医療従事者と患者の合理的な医薬品使用を指導するよう求めた。
3.使用管理の制限を厳格にした:2011年5月、国家食品医薬品監督管理局は通知を発布して、12歳以下の児童への使用を禁止し、適応症、医薬品使用量、治療期間などを制限する具体的な措置を含むニメスリド経口製剤に対する使用管理を強化した。
4.医薬品批准証明文書又は医薬品基準の撤回
(1)2011年1月、国家食品医薬品監督管理局はデキストロプロポキシフェンを含む医薬品製剤を徐々に中国市場から撤去させることを決定した。当該医薬品に対するモニタリングと研究のデータから、デキストロプロポキシフェンを含む医薬品製剤に重大な心臓に対する毒副作用が存在し、また過剰に服用すれば生命を脅かす可能性があり、中国での使用リスクが利益を上回ったことを明らかにした。2011年7月31日から、デキストロプロポキシフェンを含む医薬品製剤の生産、販売と使用を停止させ、当該医薬品に対する批准証明文書を撤回した。
(2)2011年5月、国家食品医薬品監督管理局はアルミトリンとラウバシン錠剤の中国での生産、販売と使用を停止させ、批准証明文書を撤回すると決定した。臨床研究の結果によると、その有効性が医薬品使用チームと慰安剤チームにおいて統計学における差異がなく、アルミトリンとラウバシン錠剤が有効に非痴呆性血管認知機能障害患者の認知機能を高められると認めないことを明らかにした。
(3)2011年9月、国家食品医薬品監督管理局は塩酸クレンブテロール錠剤の生産、販売と使用を停止させ、また医薬品批准証明文書を撤回した。当該品目に対する再評価は、塩酸クレンブテロール錠剤が潜在的な濫用のリスクを有し、臨床における価値が限りあり、長期間にわたる不合理な利用が患者の心肺機能に重大な影響を与えることになり、医薬品使用のリスクが利益を上回ったと考えられる。
5.医薬品生産企業との対話:2011年、医薬品不良反応モニタリングと予防接種異常反応モニタリングで見つかった一部分の生産企業の個別品目の不良反応発生率がやや高いという問題に的を絞って、国家食品医薬品監督管理局はプロゲステロン注射液などの関係企業との対話を組織した。企業に不良反応に対するモニタリングの状況を通達し、企業に真剣に原因を究明し、はやめにリスク制御の措置を制定し、品質研究を展開するよう求めた。同時に、このような状況をGMP飛行検査と追跡検査の範囲に取り入れ、地方医薬品監督管理部門に生産企業に対する監督検査を強化するよう要めた。
注解:年間報告統計データに関する説明
1.本年間報告の中のデータは、「全国医薬品不良反応モニタリングネットワーク」の中にある2011年1月1日から2011年12月31日まで各地区が報告されたデータから集計した。
2.品目ごとの医薬品不良反応/事件報告の数量は、当該医薬品の使用数量と当該医薬品不良反応の発生率などの多要因からの影響を受けている。他の自発的報告のモデルをとっている国と似ているように、中国不良反応モニタリングネットワークに収集されたデータには局限性が存在している。例えば、報告を少なめにすること、報告を漏らすこと、具体的な情報が不足することなどがあげられる。
四、結語
2011年5月、衛生部は新たに修正した「医薬品不良反応報告とモニタリング管理規則」(衛生部令第81号)を印刷・配布して、また2011年7月1日に本格的な実施を開始した。新たな規則が発布・実施されて以来、各級の医薬品監督管理部門と衛生行政部門は積極的に宣伝・トレーディングを組織し、真剣に関係要求を徹底化させてきた。社会各界の支援と協力の元、2011年の医薬品不良反応モニタリング業務は著しい成果を収めた。
2011年に、全国の末端医薬品不良反応モニタリングシステム建設は突発的な進展を収め、333の都市は医薬品不良反応モニタリング機構を設立し、専門の機構及び担当者を指定して医薬品不良反応モニタリング業務を担当させることで、医薬品不良反応モニタリング業務の突っ込んだ展開に基礎を固めた。新設した医薬品不良反応モニタリング情報ネットワークシステムも2011年に運営試行し、ネットワークの直接にカバーする範囲がますます広がり、オンライン報告の機構が持続的に増加し、モニタリングデータの全体的品質と利用可能性がが絶えぬ向上し、医薬品不良反応モニタリング事業が好調な発展のモメンタムを保ち、公衆の医薬品使用安全に有効な保障を提供した。
(出所:SFDAウェブサイト 2012年05月31日)



 ホーム
ホーム 最新情報
最新情報 機構紹介
機構紹介 国際交流
国際交流 サイトについて
サイトについて